La toxoplasmose
Qu’est-ce que la toxoplasmose ?
La toxoplasmose est une maladie infectieuse transmise par un parasite : Toxoplasma gondii. La transmission se fait via l’eau ou la nourriture contaminée par ce parasite. Cette parasitose est l’une des plus répandues dans le monde, touchant plus d’un tiers de la population mondiale.
En France, environ 30 à 50 % de la population adulte est porteuse du parasite Toxoplasma gondii. Cela signifie qu’une personne sur deux a été exposée au parasite, souvent sans symptômes, car la plupart des infections sont asymptomatiques.
Toutefois, la toxoplasmose peut être dangereuse, voire mortelle dans certains cas. En effet, elle est une cause importante de morbidité et de mortalité néonatale. La toxoplasmose concerne 1 grossesse sur 1000 en France.
Des formes graves et fatales de la toxoplasmose peuvent se déclarer chez des personnes immunodéprimées (SIDA, patients greffés ou atteints de certains cancers).
Il a également été découvert que la toxoplasmose pouvait représenter un facteur de risque dans la survenue de maladies mentales, l’infection parasitaire pouvant attaquer le système nerveux central.
Comment se transmet la toxoplasmose ?
La transmission de la toxoplasmose se fait lorsqu’une personne ingère de l’eau ou des aliments infectés par le parasite Toxoplasma gondii.
La transmission de la toxoplasmose s’opère généralement lors de :
- La consommation de viande crue ou mal cuite,
- La consommation de légumes ou d’eau contaminés,
- La grossesse, de la mère à l’enfant, via le placenta
- D’un contact avec des excréments de chat – le parasite gondii se reproduit dans l’intestin du chat.
- Contact avec des objets ou des surfaces contaminés: terre ou sable contaminés (souvent par des déjections félines). Très rarement lors d’une transfusion sanguine et transplantation d’organes.
Quels sont les symptômes de la toxoplasmose ?
Bien qu’elle soit majoritairement asymptomatique, les symptômes de la toxoplasmose bégnine sont :
- Fièvre légère
- Fatigue
- Douleurs musculaires (myalgies) et articulaires.
- Glandes lymphatiques enflées (lymphadénopathie)
- Maux de tête.
- Mal de gorge.
Dans les cas les plus graves, les symptômes sont plus localisés et prononcés. On peut alors parler de :
- Toxoplasmose oculaire : affection de la vision jusqu’à la possible perte de la vue.
- Encéphalite toxoplasmique : confusion, maux de tête graves, convulsion, fièvre élevée et paralysie partielle.
- Des complications neurologiques ont également été identifiées, pouvant mener à des maladies mentales
La forme congénitale, chez le fœtus, peut entrainer des symptômes graves :
- Retard mental ou troubles de développement neurologiques
- Problèmes oculaires (comme la rétinite, qui peut entraîner la cécité)
- Microcéphalie (petite taille de la tête, associée à des troubles du développement cérébral)
- Jaunisse et troubles du foie
- Convulsions
- Rash cutané (éruption cutanée).
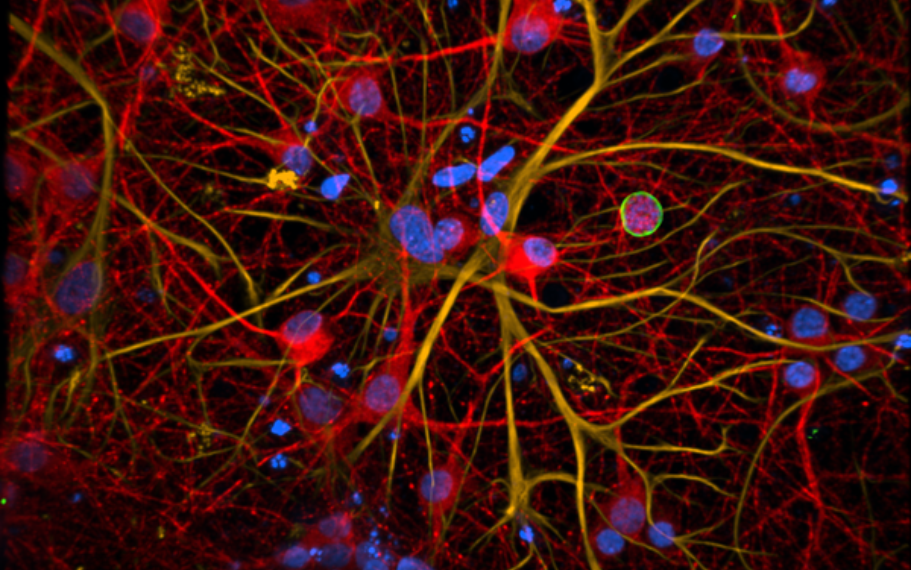
Neurones (en rouge) et cellules astrocytaires (en jaune) cultivés dans un système microfluidique et infectés par Toxoplasma gondii (kyste du parasite en vert).
©CIIL – API-B
Comment diagnostiquer la toxoplasmose ?
Le diagnostic de la toxoplasmose repose principalement sur des tests sérologiques (analyse de sang pour détecter les anticorps contre le parasite). En cas de complications, des examens médicaux plus poussés sont proposés.
Il est indispensable pour la femme enceinte de faire un diagnostic de la toxoplasmose. En France, tous les 2 à 3 mois pendant la grossesse, un dépistage sérologique est réalisé pour vérifier si la femme est immunisée contre Toxoplasma gondii (c’est-à-dire si elle a déjà été exposée au parasite avant la grossesse) ou si elle est susceptible de contracter l’infection pendant la grossesse.
Quels sont les traitements de la toxoplasmose ?
Dans la majorité des cas, le traitement contre la toxoplasmose n’est pas nécessaire. Seuls les symptômes sont traités.
Traitement de la toxoplasmose lors d’une grossesse
Lorsque la toxoplasmose est diagnostiquée chez une femme enceinte, une prise en charge immédiate en milieu hospitalier est alors activée. Un traitement par spiramycine est prescrit jusqu’au bilan en centre spécialisé.
Après le bilan,
- si le fœtus ou l’enfant est diagnostiqué avec une toxoplasmose congénitale, un traitement antibiotique est alors prescrit jusqu’à l’accouchement. Si des malformations sont détectées lors des échographies, une interruption médicale de grosse peut être envisagée.
- si le test pour la toxoplasmose congénitale est négatif, alors le traitement par spiramycine est poursuivi jusqu’à l’accouchement.
Suite à l’accouchement, dans le cas d’une toxoplasmose congénitale, le nouveau-né reçoit un traitement antibiotique par pyriméthamine-sulfamides pendant au moins un an. Une surveillance régulière est nécessaire.
Traitement de la toxoplasmose chez les personnes immunodéprimées
Si la personne est immunodéprimée et a déjà été infectée par le parasite de la toxoplasmose dans le passé, un traitement préventif peut parfois être nécessaire, généralement sous forme d’un antibiotique tel que le cotrimoxazole.
Si la personne est immunodéprimée et que certains de ses organes sont déjà affectés par le parasite, le traitement de première intention consiste en une association de pyriméthamine et de sulfadiazine, accompagnée d’un supplément d’acide folique. Une alternative possible est l’association pyriméthamine et clindamycine.
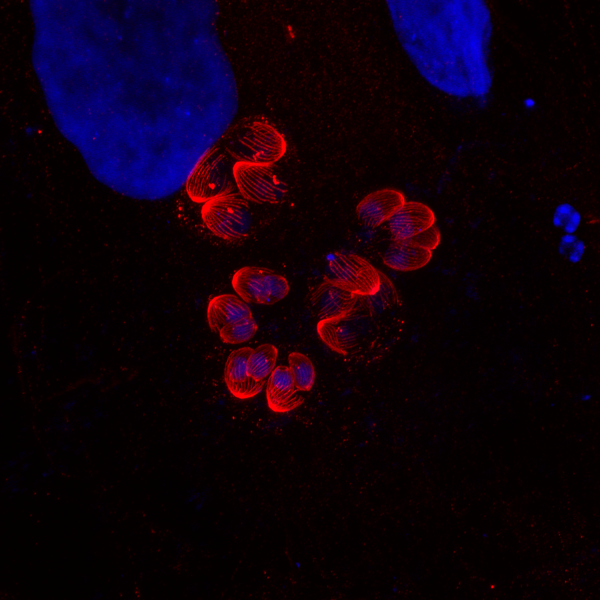
Micrographie en ultra-expansion de Toxoplasma gondii à l’intérieur d’un fibroblaste humain.
Certains parasites montrent des cellules filles en développement, tandis que d’autres assemblent l’appareil mitotique en préparation à la division.
Le bleu représente le DAPI (marquage de l’ADN), et le rouge met en évidence l’alpha-tubuline (cytosquelette et appareil mitotique).
Credits : API-B Team UMR9017/U1019 and BioImaging Center Lille
La toxoplasmose et les femmes enceintes
Les femmes enceintes doivent impérativement faire un dépistage de la toxoplasmose. En effet, cette maladie peut s’avérer très grave, voire mortelle pour son futur enfant.
Grâce à un bilan sanguin, la femme enceinte peut savoir si elle est ou non porteuse de la maladie. Auquel cas, le risque de toxoplasmose congénitale (toxoplasmose du fœtus) peut s’avérer.
Si le diagnostic de la toxoplasmose congénitale est positif, alors la mère devra suivre un traitement adapté durant toute sa grossesse en plus d’un suivi spécialisé à l’hôpital.
Prévention de la toxoplasmose, les gestes à adopter
Les femmes enceintes et les personnes immunodéprimées sont à risques élevés de contracter une forme grave de la toxoplasmose. Il n’y a pas de vaccin contre la toxoplasmose, c’est pourquoi, des gestes préventifs sont à adopter.
La prévention de la toxoplasmose inclut notamment :
- Un lavage soigneux des mains,
- Le nettoyage des fruits et légumes contaminés par la terre,
- L’évitement de certains aliments
- L’évitement du contact avec les chats.
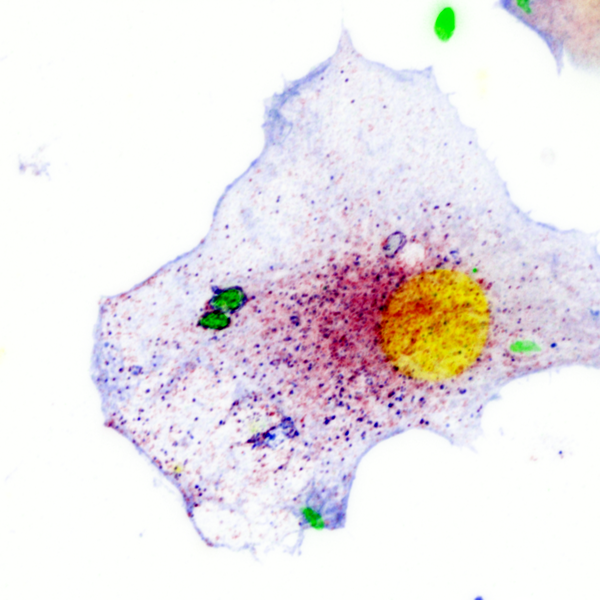
Cellule dendritique murine infectée par Toxoplasma gondii.
Peu après l’infection par plusieurs parasites (en vert), cette cellule dendritique a été capable de détecter deux vacuoles parasitophores et de les perturber, comme le montre le co-recrutement de TLR9 (en rouge) et de Galectine-3 (en bleu), visualisé en noir.
Image acquise avec le microscope confocal Zeiss Airyscan.
Jaune : noyaux (DAPI)
Vert : T. gondii-dTomato
Rouge : TLR9-GFP
Bleu : Galectine-3
©CIIL – API-B
La recherche sur la toxoplasmose à l’Institut Pasteur de Lille
Le Centre d’Infection et d’Immunité de Lille mène des recherches pour mieux comprendre et lutter contre la toxoplasmose, et plus particulièrement l’équipe Biologie des parasites Apicomplexes.
Étude sur une protéine clé du parasite Toxoplasma gondii.
Une équipe de l’Institut Pasteur de Lille a identifié une protéine clé du parasite Toxoplasma gondii qui pourrait jouer un rôle majeur dans l’infection. Cette protéine permet au parasite de se fixer aux cellules hôtes et d’envahir les tissus. La découverte pourrait ouvrir la voie à de nouvelles stratégies thérapeutiques contre la toxoplasmose, en ciblant cette protéine pour empêcher l’infection ou limiter sa propagation dans l’organisme.
La toxoplasmose et le cerveau
L’Institut Pasteur de Lille a également mené des recherches sur l’impact de Toxoplasma gondii sur le cerveau humain. L’infection par ce parasite peut entraîner des troubles neurologiques, notamment des anomalies du comportement, de la mémoire, et des troubles psychiatriques. Les chercheurs ont étudié comment le parasite affecte les neurones, et cherchent à mieux comprendre les mécanismes moléculaires sous-jacents à ces effets. Ces recherches visent à améliorer la gestion clinique de la toxoplasmose, en particulier chez les personnes immunodéprimées ou enceintes, qui sont plus susceptibles de développer des complications neurologiques graves.
Nouvelle voie d’activation dans la protection contre la toxoplasmose
Les chercheurs de l’Institut Pasteur de Lille ont identifié une nouvelle voie d’activation immunitaire qui joue un rôle important dans la protection contre la toxoplasmose. Cette découverte pourrait permettre de développer de nouvelles stratégies vaccinales ou de traitement en renforçant la réponse immunitaire de l’hôte face à l’infection. L’étude met en lumière l’importance des mécanismes immunitaires peu étudiés auparavant dans la lutte contre Toxoplasma gondii.
Régulation transcriptionnelle du cycle cellulaire asexué
Une étude clé réalisée à l’Institut Pasteur de Lille a identifié TGAP2IX-5, une protéine régulatrice de la division cellulaire asexuée dans Toxoplasma gondii. Cette découverte est cruciale pour mieux comprendre le cycle de vie du parasite, notamment la manière dont il se multiplie et s’infecte dans l’hôte. Cette recherche ouvre la voie à de nouvelles cibles thérapeutiques pour bloquer la réplication du parasite et ainsi limiter la progression de l’infection.