Rencontre avec le Dr Jérôme Vicogne, Directeur de Recherche au CNRS, pour nous parler la schistosomiase ou bilharziose, une maladie parasitaire tropicale majeure. Nous allons découvrir son ampleur mondiale et son mode de transmission très original qui dépend de mollusques d’eau douce. Le spécialise de l’Institut Pasteur de Lille nous expose la complexité du cycle de vie de ce parasite et les différentes espèces affectant l’humain. Il nous parlera aussi, des défis liés aux traitements actuels, notamment la résistance au seul médicament disponible, ainsi que l’état de la recherche sur les vaccins et de nouvelles thérapies.

Jérôme Vicogne, directeur de recherche CNRS, biochimiste et biophysicien au sein de l’équipe, “Chimie Biologie des Vers Plats (CBF)” à l’Institut Pasteur de Lille.
Jérôme Vicogne (JV) : La schistosomiase, également appelée bilharziose, est une maladie parasitaire humaine majeure, se classant comme la deuxième plus répandue au monde après le paludisme en termes d’impact socio-économique et de nombre de personnes exposées (plus de 700 millions). On appelle aussi cette parasitose la “bilharziose” en honneur du Dr Théodore Bilharz, le médecin explorateur allemand qui a établi le premier a établi lien entre la maladie et la présence de vers et d’œufs dans l’organisme en 1851.
La schistosomiase est une maladie chronique et invalidante qui touche environ 260 millions de personnes dans les régions tropicales et subtropicales, causant officiellement 30000 décès par an.
Quelle est l’ampleur de l’impact de la schistosomiase en termes de morbidité et de mortalité ?
JV : La schistosomiase est une maladie chronique et invalidante qui touche environ 260 millions de personnes dans les régions tropicales et subtropicales, causant officiellement 30000 décès par an. Cependant, le nombre réel de décès pourrait être bien plus élevé, officieusement estimé à plus de 300 000 par an, voire davantage. Cette sous-estimation est due au fait que la mort n’est pas souvent directement imputable à la bilharziose elle-même, mais aussi aux autres maladies aggravées par l’infection parasitaire et leurs complications. Cette parasitose méconnue du grand public occidental entraîne pourtant un impact socio-économique majeur dans les pays d’endémie.
Comment la schistosomiase est-elle transmise à l’homme ?
JV : La schistosomiase est une maladie hydrique, c’est-à-dire qu’elle est transmise lors d’une baignade dans l’eau douce. Le parasite responsable, un ver plat du genre Schistosoma, a besoin d’un mollusque d’eau douce (un escargot) comme hôte intermédiaire pour réaliser une partie du cycle de reproduction. L’homme est infecté lorsque des larves infectieuses, appelées cercaires, sont libérées par les mollusques dans l’eau. Les cercaires pénètrent activement à travers la peau en quelques minutes lors d’un simple contact avec de l’eau contaminée (baignade, lavage, activités agricoles, etc.). Pas besoin de la boire pour s’infecter !
Existe-t-il différentes espèces de Schistosoma et quelle est leur répartition géographique ?
JV : Il existe de nombreuses espèces de Schistosomes qui peuvent infester divers mammifères et oiseaux, mais seulement cinq sont capables d’infecter l’homme. Ces espèces ont une répartition géographique distincte : Schistosoma mansoni, Schistosoma haematobium et Schistosoma intercalatum sont principalement présentes en Afrique. S. mansoni est également présent en Amérique du Sud, où il a été introduit par les Européens et probablement lors de la traite des esclaves au XVI siècle. Schistosoma japonicum et Schistosoma mekongi sont des espèces typiquement asiatiques. Schistosoma haematobium et Schistosoma mansoni peuvent également être trouvées au Proche-Orient, notamment dans les oasis et les zones humides. La présence de ces espèces est strictement conditionnée par la distribution des mollusques hôtes, spécifiques à chaque espèce de schistosomes, et aussi par les migrations humaines et animales.
Quels sont les symptômes de la schistosomiase et comment évolue la maladie ?
JV : Les symptômes de la schistosomiase varient en fonction du niveau d’infestation, du stade de l’infection et de l’espèce de Schistosome impliquée. On distingue généralement trois phases. La phase aiguë (ou de contamination) se manifeste rapidement de la pénétration des cercaires dans la peau, une dermatite peut apparaître (petits points rouges, démangeaisons). Quelques jours ou semaines plus tard, une réaction systémique appelée fièvre de Katayama peut survenir, souvent associée à une toux sèche (due au passage des parasites dans les poumons), des douleurs musculaires et de la fatigue. Certaines personnes peuvent ne présenter aucun symptôme initial. La phase chronique précoce correspond à l’établissement des vers adultes dans les veines autour des intestins ou de la vessie, au début de la ponte des œufs et à leur passage au travers des tissus. Les symptômes peuvent inclure des douleurs abdominales, des diarrhées, la présence de sang dans les urines (hématurie, plus fréquente dans l’infection à S. haematobium), et des mictions fréquentes. Durant la phase chronique tardive, les œufs qui ont été transportés par la circulation sanguine et piégés dans divers tissus, provoque une inflammation chronique ; notamment du foie (granulomes bilharziens), avec une évolution rapide en une fibrose et hépatosplénomégalie (gonflement du foie et de la rate), et à terme, l’installation d’une hypertension portale avec risque de rupture de varices œsophagiennes, pouvant être fatale. L’affaiblissement généralisé (cachexie), l’augmentation des risques de cancers de la vessie et du foie, mais aussi les complications associées à d’autres infections sont souvent des causes indirectes de décès.
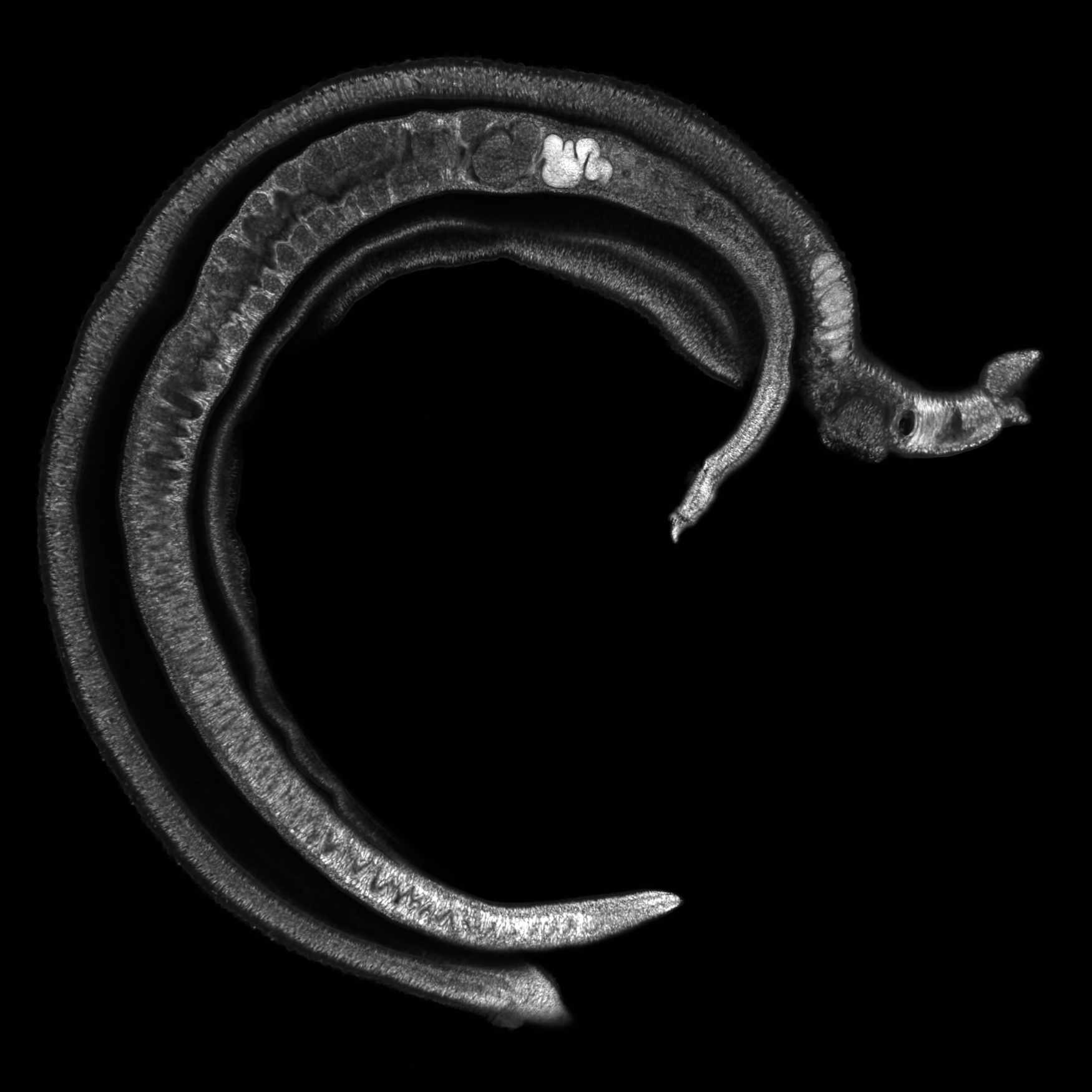
Couple de schistosomes adultes au microscope confocal. On voit la femelle à l’intérieur du canal Gynecophore du mâle
Quels sont les traitements et où en est la recherche sur les vaccins contre la schistosomiase ?
JV : Actuellement, le principal médicament pour traiter la schistosomiase est le Praziquantel. Il est efficace contre toutes les espèces de Schistosome et a révolutionné la prise en charge de la maladie depuis les années 1980 grâce à son efficacité en une seule dose et ses faibles effets secondaires. Cependant, son utilisation massive et parfois détournée (notamment pour traiter le bétail) a conduit à l’émergence de souches de parasites moins sensibles, voire résistantes, ce qui représente une préoccupation majeure. La recherche de nouvelles molécules thérapeutiques est en cours, mais elle est complexe en raison des difficultés de transposer les résultats obtenus in vitro à la réalité in vivo.
Concernant les vaccins, un essai clinique prometteur (Bilhvax) basé sur les études réalisées à l’IPL n’a malheureusement pas donné les résultats escomptés lors des phases 3. Actuellement, trois autres essais cliniques sont en cours, dont un (Sm-p80) semble être le plus prometteur. Le développement d’un vaccin reste néanmoins très difficile par la capacité du Schistosome à moduler et échapper au système immunitaire de l’hôte vertébré.
Le changement climatique et les migrations ont-ils un impact sur la propagation de la schistosomiase ?
JV : Oui, le réchauffement climatique et les migrations humaines sont des facteurs qui favorisent l’émergence et la propagation de la schistosomiase dans de nouvelles zones géographiques. C’est de cette manière que le parasite a conquis toute la planète. Le réchauffement climatique permet à des mollusques hôtes potentiels, y compris des espèces invasives, d’étendre leur aire de répartition vers des latitudes plus élevées. Les migrations humaines et animale peuvent introduire le parasite dans des régions où le mollusque hôte compatible est présent, comme cela a été observé en Corse en 2014 et 2015. La combinaison de ces deux facteurs augmente le risque d’apparition de la schistosomiase dans des zones auparavant non endémiques.
Quelles sont les perspectives de recherche actuelles sur la schistosomiase au-delà du développement de nouveaux médicaments et vaccins ?
La recherche actuelle sur la schistosomiase explore diverses pistes qui vont de l’immunologie à la biologie animale. Une première approche est de comprendre l’interaction parasite-hôte, notamment étudier comment le Schistosome se déplace et de repère dans le corps, comment les couples mâle-femelle se forment et interagissent in vivo, et comment le parasite interagit avec les tissus, en particulier le foie et les vaisseaux sanguins, au niveau moléculaire et cellulaire. Le développement de modèles d’organes sur puce permet de mieux mimer l’environnement physiologique du parasite. La seconde approche consiste à étudier le rôle des œufs dans la pathogénèse pour comprendre comment ils provoquent l’inflammation et la fibrose, et comment cette réaction pourrait être modulée. Il faut également rechercher de nouvelles cibles thérapeutiques en identifiant des mécanismes essentiels à la survie et à la reproduction du parasite qui pourraient être bloqués par de nouvelles molécules. Il faut également explorer le potentiel immunomodulateur du parasite, étudier comment les vers adultes parviennent à échapper au système immunitaire de l’hôte pendant des dizaine d’année. Ces propriétés uniques d’immunosuppression, pourraient être exploitées pour contrôler d’autres maladies inflammatoires ou auto-immunes. Enfin, il faut aussi valoriser les connaissances de la médecine traditionnelles, en particulier les plantes médicinales utilisées dans les zones d’endémie pour identifier de potentielles molécules antiparasitaires. La collaboration entre différentes disciplines (biologie, chimie, médecine, sciences humaines) est donc essentielle pour progresser dans la lutte contre cette maladie tropicale négligée (NTD).
L’éradication de la schistosomiase est possible, comme le montre l’exemple du Japon qui y est parvenu grâce à une lutte intégrée (lutte antivectorielle, modifications environnementales, éducation, mécanisation et utilisation de produits chimiques) avant même l’arrivée du Praziquantel Cependant, une telle approche est plus complexe à l’échelle d’un continent. Pour Jérôme Vicogne, la priorité est de trouver rapidement une alternative au Praziquantel en raison de l’émergence de souches résistances. Le développement d’un vaccin reste un objectif important, malgré les immenses défis posés par la capacité du parasite à échapper au système immunitaire. L’espoir existe car des vaccins efficaces commencent à être administrés pour d’autres maladies parasitaires majeure comme le paludisme.
Il est donc crucial d’informer les populations et de sensibiliser à cette maladie tropicale négligée. Le laboratoire de Lille est l’un des rares en Europe à maintenir un cycle complet du parasite, ce qui est essentiel pour la recherche. Pourtant, les financements pour la recherche sur le schistosome sont limités et sans le soutien de l’IPL cette recherche serait impossible. L’entretien des élevages de mollusques est coûteux en ressources humaines et financières. La perte du cycle serait très difficile à surmonter si on souhaite maintenir une recherche originale qui vise à la fois à comprendre les mécanismes d’interaction entre le parasite et son hôte, dans l’espoir de développer de nouveaux médicaments, et à développer de nouvelles approches pour soigner des maladies hépatiques et inflammatoires.
