Nouvelle piste dans la lutte contre la chimiorésistance des cellules cancéreuses coliques
Le cancer colorectal, regroupant les cancers du côlon et du rectum, est une des formes de cancer les plus courantes dans le monde. En France il constitue la troisième cause la plus fréquente de cancer et la deuxième cause de décès par cancer. Chaque année, environ 43 000 nouveaux cas sont diagnostiqués dans le pays, avec une mortalité annuelle de près de 17 000 personnes. Un défi majeur dans le traitement des cancers colorectaux avancés est l’apparition de chimiorésistance, un phénomène où les cellules cancéreuses deviennent résistantes aux traitements. Les mécanismes de chimiorésistance incluent des changements génétiques et épigénétiques, des altérations métaboliques, et l’activation de voies de signalisation favorisant la survie des cellules cancéreuses.

Vanessa Dehennaut, Professeure des Universités et chercheuse au sein de l’équipe “Sénescence, fibrose et cancer” du laboratoire Hétérogénéité, Plasticité et Résistance aux Thérapies des Cancers (CANTHER) étudie notamment le rôle d’une voie métabolique, la O-GlcNAcylation, dans l’induction et l’échappement à la sénescence des cellules cancéreuses coliques en réponse à la chimiothérapie, un mécanisme impliqué dans la résistance aux traitements anticancéreux et à la récidive de la maladie.
Votre étude publiée dans Cell Death and Disease a identifié une voie métabolique dont l’inhibition permettrait d’empêcher l’apparition de certaines chimiorésistances. Cela pourrait-il constituer une avancée dans la prise en charge des patients ?
Vanessa Dehennaut : Ce projet qui représente 4 ans de recherche a permis d’identifier un mécanisme impliquant une voie métabolique particulière appelée O-GlcNAcylation qui contribue à la résistance des cellules cancéreuses coliques face à de faibles doses de chimiothérapie. C’est vraiment la première fois qu’est mise en évidence cette voie métabolique impliquée dans le phénomène de la résistance à la chimiothérapie et via la sénescence de ces cellules. L’objectif principal est de développer de nouvelles approches thérapeutiques afin d’améliorer l’efficacité des traitements, et de réduire leurs effets secondaires.
Cette technique de culture d’organoïdes est novatrice mais coûteuse, car elle nécessite des milieux spécifiques et des facteurs de croissance. C’est pourquoi la recherche a besoin de financement.
Quelles sont les prochaines étapes de vos recherches ?
VD : La prochaine étape est l’utilisation d’organoïdes dérivés de tumeurs de patients qui conservent les caractéristiques génétiques de la tumeur d’origine, et sont plus représentatifs des situations réelles que les cultures cellulaires classiques utilisées en laboratoire. Il nous est possible d’obtenir des échantillons qui sont prélevés de la tumeur des patients que nous remettons en culture, nous permettant ainsi de disposer d’un panel de « tumoroïdes » avec le profil génétique de chaque patient. Cette technique de culture d’organoïdes est novatrice mais coûteuse, car elle nécessite des milieux spécifiques. C’est pourquoi la recherche a besoin de financement.
Quelles sont les perspectives pour les patients ?
VD : A terme, nous souhaitons nous diriger vers un essai clinique, car nous pensons que cette avancée apporte un nouvel espoir de pouvoir combiner des faibles doses de chimiothérapie avec des inhibiteurs de la O-GlcNAcylation en réduisant ainsi les effets secondaires pour le patient pendant traitement, et à plus long terme d’empêcher l’apparition de la chimiorésistance et de pouvoir ainsi guérir le cancer dès le traitement de première ligne.

Illustration : La partie gauche de la figure montre qu’au sein d’une tumeur, toutes les cellules ne reçoivent pas les mêmes doses de chimio : celles qui reçoivent les plus fortes doses meurent par apoptose et celles qui reçoivent des doses plus faibles entrent en sénescence. La sénescence est un état cellulaire particulier dans lequel les cellules sont caractérisées par des changements de morphologies (elles deviennent plus grosses) et des changements moléculaires dont un arrêt de prolifération et une reprogrammation métabolique. Le problème est que cette sénescence n’est pas stable. Certaines cellules cancéreuses sénescentes sont capables d’échapper à cet état, prolifèrent de nouveau et peuvent donc participer à la récidive de la maladie. La partie droite montre que lorsque qu’on combine de la chimiothérapie à faible dose avec des inhibiteurs de o-glcnacylation, on empêche les cellules cancéreuses d’entrer en sénescence et on induit leur mort.
Pour aller plus loin : Relation en nutrition et épigénétique* : l’implication d’un sucre dans le cancer colorectal mise en évidence
L’article de Cell death and Disease décrit plus haut fait suite aux précédents travaux dans lesquels Vanessa et son équipe avaient montré le rôle du sucre dans la carcinogenèse colique, en lien avec la nutrition et l’épigénétique. Ces travaux avaient amené les chercheurs à émettre l’hypothèse qu’inhiber ce sucre pouvait être une nouvelle cible thérapeutique potentielle.
S’il est admis depuis de nombreuses années que la nutrition peut influencer les modifications épigénétiques se produisant dans les cancers coliques, les mécanismes sous-jacents n’étaient pas jusqu’à présent entièrement connus. L’équipe du Pr Vanessa Dehennaut a mis en évidence l’implication d’un sucre synthétisé par voie métabolique appelée O-GlcNAcylation, et dont l’abondance un senseur de l’état nutritionnel de notre organisme.
Fort est de constater que la quantité de O-GlcNAcylation est anormalement élevée dans le cas d’un cancer colorectal, les travaux menés au sein de l’équipe par Amélie Decourcelle ont fait l’objet en 2020 d’une publication dans laquelle il est démontré sur un modèle préclinique in-vivo que la O-GlcNAcylation représente un lien entre la nutrition et la régulation épigénétique lié à la baisse d’un des gènes suppresseurs de tumeurs clés, UNC5A, régissant la carcinogenèse du côlon. C’est ainsi un des mécanismes de modification de l’expression des gènes par des enzymes de l’épigénétique qui vient d’être mis en évidence. Ces recherches démontrent une fois de plus d’importante d’une bonne alimentation avec une consommation en sucre raisonnée, associée à une activité sportive pour lutter contre la maladie.
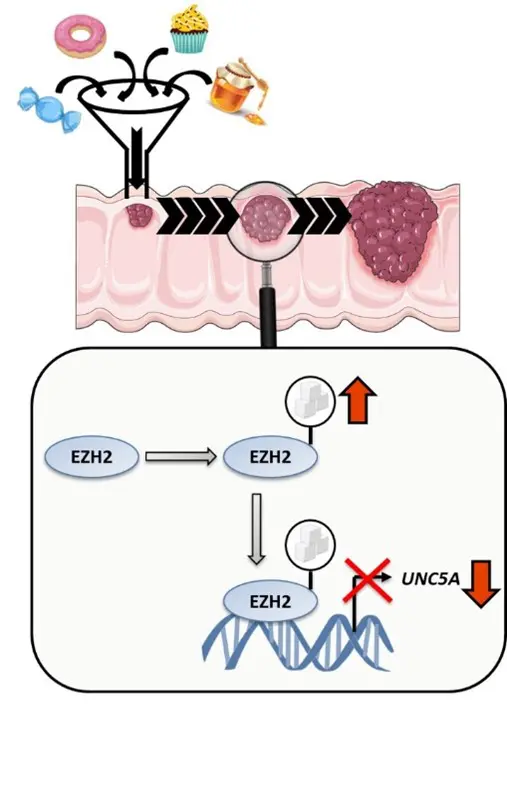
Schéma symbolisant la fixation du sucre sur l’enzyme EZH2 au niveau des cellules colorectales (au centre), et l’action de la combinaison des deux sur la baisse du gène UNC5A suppresseur de tumeurs, conduisant à un cancer (à droite).
*L’épigénétique est la discipline de la biologie qui étudie la nature des mécanismes modifiant l’expression des gènes. Les facteurs environnementaux (alimentation, maladies, médicaments et toxiques, stress, lieu et hygiène de vie) ont une influence sur notre génome par des modifications dites épigénétiques.
