Le cancer, rappelons-le, est une maladie dans laquelle les cellules continuent de se diviser et de se développer de manière incontrôlée, généralement à cause de mutations ou d’altérations moléculaires complexes de certains gènes. Les produits de ces gènes, des protéines impliquées dans des fonctions cellulaires importantes, sont alors activés, ce qui conduit à la transformation des cellules et au développement des tumeurs cancéreuses qui envahissent progressivement les tissus.

Diagnostic moléculaire des cancers : un portrait-robot plus précis des tumeurs
Dans le cancer du poumon, le cancer du sein, ou dans le mélanome par exemple, de nombreuses mutations génétiques à l’origine du développement de la maladie ont été identifiées. De façon importante, le produit de ces gènes mutés peut être ciblé spécifiquement par de nouvelles thérapies. Ces thérapies dites ciblées offrent un véritable espoir pour beaucoup de patients. Les mutations répertoriées dans les cancers sont très diverses et sont donc différentes d’un cas à l’autre. Il est donc important, en plus du diagnostic classique, qui détermine le type de cancer dont est atteint un patient, de réaliser un diagnostic moléculaire afin de faire état du type de mutation dont il est porteur. L’objectif est ensuite de pouvoir prescrire au patient une thérapie ciblée, adaptée à la mutation à l’origine de son cancer. Cette démarche s’inscrit dans la démarche de médecine de précision et pourrait notamment améliorer la prise en charge.
Le diagnostic moléculaire des cancers nécessite le séquençage de l’ADN des tumeurs sur l’ensemble des gènes susceptibles d’être mutés dans un type de cancer donné, représentant plusieurs dizaines de milliers de bases d’ADN. C’est le développement de nouvelles technologies de séquençage de l’ADN, les séquençages haut-débits, qui ont permis ces dernières années la mise en place à grande échelle du diagnostic moléculaire des cancers. Ces séquençages sont réalisés par des plateformes de biologie moléculaire dédiées comme celle du CHU de Lille. Au-delà de leur grande capacité de séquençage, ces technologies sont de plus en plus rapides et de plus en plus fiables. Certaines solutions technologiques permettent de séquencer en routine clinique, plus de 300 gènes simultanément, pour plusieurs patients.
Le séquençage de plus en plus systématique de l’ADN des tumeurs, en plus de permettre le diagnostic des mutations génétiques déjà connues, permet actuellement la découverte de nombreuses mutations dont le rôle dans le cancer n’est pas encore identifié. L’un des enjeux actuels est de savoir si ces mutations nouvellement identifiées sont ou ne sont pas des facteurs de risque de développement des cancers. En d’autres termes, l’enjeu à cette étape est moins la découverte de nouvelles mutations que leur interprétation. C’est dans ce contexte qu’à l’Institut Pasteur de Lille, l’équipe du Dr David Tulasne de l’unité CANTHER (Hétérogénéité, Plasticité et Résistance aux Thérapies des Cancers) cherche à interpréter le rôle des mutations touchant les gènes impliqués dans la prolifération anormale des cellules. Ces travaux requièrent des collaborations étroites avec les services cliniques et la mise en place en laboratoires de modèles complexes reconstituant les mutations des patients. Les travaux décrits ci-après avec le cancer du rein et la découverte de nouvelles mutations activatrices constituent un exemple concret du lien qui unit la recherche, le diagnostic d’un cancer, et la perspective de développement des nouveaux traitements.

De nouvelles mutations du récepteur MET découvertes chez des patients atteints d’un cancer du rein.
Nous avions déjà présenté les avancées réalisées à l’Institut Pasteur de Lille par l’équipe du Dr David Tulasne dans la recherche de thérapies ciblées visant les récepteurs à l’activité tyrosine kinase (RTK), afin de traiter certains cancers du poumon, notamment chez les patients présentant des mutations modifiant le récepteur MET. Le Dr Marie Fernandes (unité CANTHER – équipe Target) nous explique que de nouveaux variants germinaux de MET ont été identifiés récemment dans des familles dont plusieurs membres présentaient un cancer du rein.
Ces mutations ont été identifiées par des chercheurs et médecins spécialisés dans le diagnostic moléculaire en oncologie au sein de l’Institut Gustave Roussy à Villejuif. En collaboration, l’équipe lilloise a développé un certain nombre de tests fonctionnels afin de déterminer si la mutation identifiée est activatrice et pourrait ainsi être à l’origine du cancer. Cette information permet d’apporter un suivi particulier aux familles porteuses de cette mutation mais également d’adapter leur prise en charge par l’utilisation potentielle de traitements ciblant spécifiquement le récepteur MET.
Ces recherches ont permis de prouver qu’une des mutations présente dans une famille développant une forme particulière de cancer du rein, signature des altérations MET, était bien une mutation activatrice, modifiant de ce fait la prise en charge de ces patients, mais aussi de leurs descendants. En effet, s’ils sont porteurs de cette mutation dans leur organisme, ils sont potentiellement plus à risque de développer un cancer du rein mais qui pourrait alors être traité dès les premiers stades d’évolution par des inhibiteurs de MET.
Sources bibliographiques :
- « Le récepteur Met fête ses 30 ans : De la découverte d’un oncogène au développement de thérapies ciblées », Montagne et al., 2014. DOI : https://doi.org/10.1051/medsci/20143010013
- « Novel germline MET pathogenic variants in French patients with papillary renal cell carcinomas type I », Sebai et al., 2021. DOI : 10.1002/humu.24313.
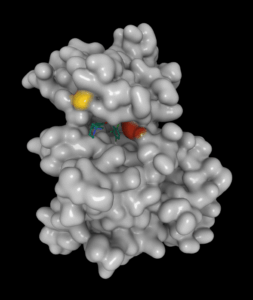
Représentation 3D du domaine à activité kinase du récepteur MET avec les acides aminés H1112 (en jaune) et Y1248 (en rouge), deux sites modifiés dans certains cancers du rein et dont la mutation conduit à l’activation dérégulée du récepteur. Il est également représenté le crizotinib, une molécule capable d’inhiber spécifiquement l’activité kinase dans la poche ATP du récepteur.
CANTHER : le centre de précision dédié aux cancers
La recherche scientifique en cancérologie sur le campus de l’Institut Pasteur de Lille est effectuée au sein de l’Unité Mixte de Recherche CANTHER – Hétérogénéité, Plasticité et Résistance aux Thérapies des Cancers – Cette unité a pour objectif principal de mieux comprendre les mécanismes de résistance aux traitements des cancers et favorise le dialogue entre les équipes cliniques et les équipes de recherche afin d’identifier de nouvelles cibles de traitements en cancérologie.
Cette compréhension des mécanismes devra ensuite mener à l’identification de nouvelles cibles thérapeutiques et de nouveaux marqueurs de la résistance, afin de pouvoir proposer aux patients atteints de cancer des thérapies adaptées et mieux ciblées. L’unité est composée de 5 équipes de chercheurs qui ont développé des expertises, des compétences et des savoir-faire spécifiques et complémentaires afin de répondre à ces objectifs : l’équipe du Dr Van Seuningen est spécialisée dans les mécanismes de résistance aux chimiothérapies, l’équipe du Dr Tulasne en collaboration avec le Dr Duterque, dans les mécanismes de résistance aux thérapies ciblées, l’équipe du Pr Le Bourhis dans les mécanismes de résistance associés au processus métastatique, l’équipe du Pr Abbadie dans les mécanismes de sénescence et de fibrose associés à la résistance et l’équipe du Pr Quesnel dans les mécanismes de dormance tumorale.
ONCOLille, 250 chercheurs et cliniciens pour lutter contre les cancers
A Lille, l’Institut de Recherches Interdisciplinaires en Cancérologie de Lille, ONCOLille, réunit plus de 250 chercheurs et cliniciens issus d’équipes pluridisciplinaires sur un thème central de recherche : la résistance aux traitements et la dormance tumorale. Soutenues par l’Institut Pasteur de Lille, les équipes de recherche des Dr David Tulasne et Martine Duterque apportent leur expertise au sein de l’institut ONCOLille. Une dynamique essentielle pour mieux comprendre la résistance aux thérapies, la dormance tumorale, les rechutes et les cancers à mauvais pronostic, tout ceci au bénéfice du patient. Cette résistance, qui peut avoir des formes multiples, est très souvent la cause de l’échec des thérapies actuelles. C’est cette résistance, par la connaissance des mécanismes, que chercheurs et les cliniciens chercheront à combattre et/ou à détourner afin de rendre de nouveau la tumeur sensible aux traitements, de proposer de nouveaux traitements par le développement de nouvelles molécules thérapeutiques et/ou par la proposition de nouvelles combinaisons de drogues et le développement de nouvelles technologies pour traiter les cancers.
En effet, le but ultime de ces recherches est de proposer une médecine personnalisée, un meilleur suivi et une meilleure prise en charge des maladies cancéreuses et de leurs conséquences.
Itinéraire d’un chercheur
Zoulika Kherrouche, chargée de recherche
Equipe TARGET- Unité CANTHER « Cancer Heterogeneity, Plasticity and Resistance to Therapies »
UMR9020 CNRS – U1277 Inserm – Université de Lille – CHU de Lille – Institut Pasteur de Lille
Originaire de Croix dans les Hauts-de-France, Zoulika souhaitait faire des études courtes pour entrer rapidement dans la vie active, et a hésité entre les beaux-arts et les sciences. Elle finira par opter pour un baccalauréat technologique STL, suivi d’un BTS biotechnologie. Elle candidate pour un poste en recherche en cancérologie à l’Institut Pasteur de Lille dans le service dirigé à l’époque par le Pr Stéhelin et travaillera avec le Pr Jean Rommelaere sur les parvovirus, puis sur la régulation de l’expression des oncogènes ETS avec le Dr Jean Coll. La passion communiquée par ses ainés la pousse à reprendre ses études. Zoulika obtient son diplôme d’ingénieur en formation continue, et rejoint l’équipe du Pr Yvan Delaunoit qui, à son tour, l’encouragera à faire une thèse. Zoulika part ensuite en post-doctorat à l’Université du Queensland en Australie où elle travaillera sur la carcinogenèse cutanée. De retour à l’Institut Pasteur de Lille, Zoulika rejoint l’équipe du Dr David Tulasne pour étudier les récepteurs à activité tyrosine kinase fréquemment mutés dans les cancers. Sa collaboration avec le Pr Alexis Cortot, Chef du service d’oncologie thoracique du CHU de Lille, l’incite à développer une recherche translationnelle pour identifier les mutations responsables de cancer pulmonaire et les mécanismes de résistance aux traitements. Après avoir passé plus de 20 ans en recherche fondamentale, Zoulika développe aujourd’hui des projets de recherche pré-clinique et translationnelle en interaction étroite avec les services hospitalo-universitaires du CHU de Lille, avec pour objectif de favoriser le transfert des connaissances obtenues en recherche fondamentale vers le développement d’essais cliniques. Elle participe également depuis une dizaine d’années à la formation par la recherche de jeunes médecins oncologues, pneumologues, anatomo-pathologistes ou chirurgiens !
« Faire de la recherche c’est l’assurance de ne jamais s’ennuyer, de rencontrer des personnes passionnées et avec beaucoup de travail et un zeste de patience, réaliser des découvertes qui améliorent la vie des patients atteints de cancer. »