Maladies émergentes et antibiorésistance : un programme innovant face à ces deux phénomènes alarmants
Si les progrès en matière d’hygiène et de vaccination ont permis de fortement limiter l’impact de ces maladies, ces dernières décennies ont été marquées par une accélération alarmante de l’émergence de nouveaux agents infectieux au sein des populations humaines. L’épidémie de Covid-19 a rappelé la nécessité d’agir face à ces menaces émergentes car malheureusement, de nouvelles menaces arrivent…
Un autre phénomène inquiétant provient de la résistance croissante des nombreuses bactéries aux antibiotiques dont l’usage, trop souvent systématique et parfois inapproprié, a conduit à l’apparition de souches multi-résistantes. Les échecs des thérapies actuelles contre la tuberculose, première cause de mortalité dans le monde par maladie infectieuse, en est l’exemple le plus marquant. L’ ampleur du problème est telle que l’antibiorésistance est aujourd’hui considérée par l’Organisation Mondiale de la Santé comme l’une des plus graves menaces pesant sur la santé mondiale.

La France demeure un pays sur-consommateur d’antibiotiques et apparaît comme l’un des pays européens les plus touchés par la résistance des agents infectieux aux antibiotiques. La multirésistance aux antibiotiques est donc un problème majeur de santé publique dans notre pays.
Aujourd’hui, le défi de taille est de contrer rapidement deux phénomènes alarmants : le développement de nouvelles épidémies et la résistance des maladies infectieuses aux antibiotiques.
Alors comment lutter contre les maladies infectieuses à l’ère de l’antibiorésistance ?
Combattre les maladies infectieuses est une mission historique de l’Institut Pasteur de Lille depuis plus de 120 ans. Aujourd’hui, en rassemblant une masse critique de scientifiques associant de façon complémentaire et synergique l’ensemble des expertises nécessaires, l’Institut Pasteur de Lille s’est donné pour objectif d’identifier de nouveaux principes thérapeutiques contre les infections virales émergentes et les infections par des bactéries multi-résistantes.
Maladies infectieuses émergentes : identifier de nouveaux principes thérapeutiques
Beaucoup de maladies infectieuses émergentes sont des zoonoses(1) dont l’agent d’origine animale, le plus souvent un virus, a franchi la barrière d’espèces pour atteindre l’homme. Parfois, un réarrangement de gènes ou des mutations du génome microbien génèrent de nouveaux agents capables de se transmettre d’homme à l’homme. Enfin, la perturbation des écosystèmes peut favoriser la ré-émergence de parasites et de pathogènes bactériens ou fongiques connus, entraînant l’apparition d’épidémies synergiques.
D’après l’Organisation Mondiale de la Santé Animale, 60% des maladies infectieuses humaines sont zoonotiques.

Le Pr Benoit Deprez, directeur de l’U1177 “Drugs & Molecules for Living Systems”, et le Dr Julie Charton, pharmacienne spécialisée en chimie médicinale, mènent à l’Institut Pasteur de Lille avec leurs équipes des travaux pour élargir les recherches à la famille des Coronavirus, au-delà de SARS-CoV-2.
Ce dernier reste un vrai problème de santé publique, car même en présence de vaccins, disposer de médicaments demeure très important, or les premiers médicaments qui vont arriver sur le marché, comme le Molnupiravir par exemple, sont encore améliorables. Le besoin thérapeutique reste existant, avec l’obligation de ne plus être dans la passivité face à ces menaces émergentes, mais de disposer au contraire d’un arsenal préparé pour lutter contre ces maladies infectieuses.
Le projet Pan-Coronavirus a pour objectif d’identifier des molécules qui vont être actives de façon la plus large possible sur la famille des Coronavirus dont le réservoir animal est gigantesque. La diversité dans ce réservoir, estimée à plus d’un millier, est telle que la probabilité qu’un virus repasse de l’animal à l’homme est inéluctable. « Plus nous avons d’interactions avec les biotopes naturels (par l’exploration de forêts profondes, par les contacts avec des animaux sauvages, et principalement des mammifères…), plus nous avons de chance qu’une transmission fortuite se réalise » rappelle le Pr Deprez.
Depuis le début de la mobilisation de l’Institut Pasteur de Lille contre la pandémie à SARS-Cov-2, les équipes travaillent sur une approche rapide (Cf. projet THERAPIDE), et sur une approche à plus long terme ciblant une protéase commune à l’ensemble de ces virus. Cette protéase est une fonction très conservée au sein des virus de cette famille, on peut donc obtenir un même effet d’un Coronavirus à l’autre en inhibant la fonction de cette protéase. Les premières avancées réalisées ont déjà fait l’objet d’une publication dans la prestigieuse revue « Angewandte Chemie » (en allemand : chimie appliquée). Cette publication décrit une partie nouvelle de description de la protéase par la RNM (Résonnance Magnétique Nucléaire), et l’interaction avec des molécules qui ont été découvertes au laboratoire.
Bibliographie : Angew Chem Int Ed Engl. 2021 Sep 27. doi: 10.1002/anie.202109965.
100.000 molécules ont été criblées et plusieurs familles de composés actifs identifiées que les chercheurs sont en train d’optimiser avec les outils de la chimie médicinale. Trois unités de recherche collaborent sur ce projet, rassemblant de nombreuses compétences. Deux post-doctorats et deux doctorants travaillent actuellement sur la chimie, un ingénieur d’étude a été embauché pour une durée de 18 mois afin d’étudier l’enzymologie et activité vitro, un post-doctorat en modélisation moléculaire est attendu au mois de novembre. Dans l’équipe de biologie structurale de Xavier Hanoulle, un ingénieur a été recruté pour établir toute la biologie structurale.

Bien sûr toutes les recherches menées par l’équipe du Pr Jean Dubuisson, directeur du Centre d’Infection et d’Immunité de Lille, sur SARS-Cov-2 et les outils mis en place pour ce virus vont être capitalisés pour ce nouveau projet. Les travaux sur la protéase sont d’ores et déjà menés sur SARS-Cov-2, mais aussi d’autres Coronavirus déjà existants. La modélisation moléculaire va permettre d’anticiper le spectre d’utilisation des produits à l’ensemble des Coronavirus. Basés sur le développement de nouveaux médicaments et non plus par repositionnement d’anciennes molécules, ces travaux, menés grâce au soutien de nos donateurs, nécessiteront au moins 24 mois de recherche pour voir de réelles avancées et identifier un candidat médicament qui pourra passer en développement pré-clinique et clinique.
Antibiorésistance : le cas concret de la tuberculose
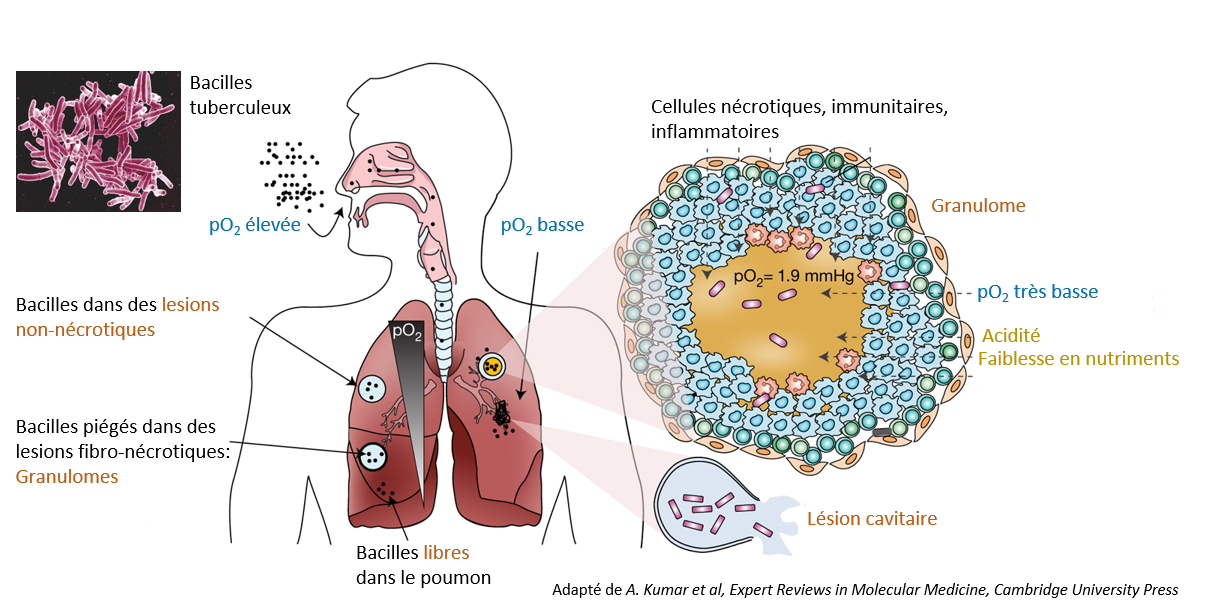
L’antibiorésistance est un autre phénomène très préoccupant pour notre santé, car si les antibiotiques constituent une des découvertes les plus importantes de la médecine qui a sauvé et qui sauve encore des millions de vies chaque année, leur efficacité est menacée car les bactéries peuvent s’adapter et résister au traitement. Un exemple concret est celui de la tuberculose. La tuberculose est une maladie infectieuse grave, souvent mortelle, due à un bacille (Mycobacterium tuberculosis) qui infecte le plus souvent les voies respiratoires et les poumons mais qui peut également atteindre d’autres organes, et même se loger dans certaines cellules à l’état de dormance, ce qui explique la pratique d’une polythérapie pour son traitement. C’est une maladie fortement transmissible par voie aérienne, par dispersion de gouttelettes de secrétions bronchiques provenant d’un malade contagieux.
La tuberculose tue plus dans le monde que toute autre maladie infectieuse.
1,4 million de personnes dans le monde décédées de la tuberculose en 2019.
Le premier traitement, la Streptomycine, a été découvert en 1946 et utilisé de façon généralisée dans les années 50. Cependant, dès les premières utilisations, les premières souches résistantes ont émergé. La période allant de 1950 à 1963 a vu naître l’ensemble des traitements anti-tuberculeux encore en usage aujourd’hui. On finira par utiliser ces antibiotiques dans une polythérapie plus ou moins efficace, parce que pratiquée de façon peu rationnelle et sans fondement scientifique par simple empilement. Cette pratique va créer un « cocktail » qui n’est pas optimum et qui ne touche pas à toutes les formes de tuberculose, notamment celles qui se cachent en dormance dans les macrophages(2), et va induire un phénomène d’antibiorésistance.
Pour comprendre les raisons de l’échec des thérapies actuelles de la tuberculose résistante, le Dr Baulard explique que les bactéries adoptent des physiologies très différentes en fonction de l’endroit où elles se trouvent dans le corps de leur hôte. De plus, la plupart des antibiotiques ne sont actifs que sur des bactéries qui se divisent, et non lorsqu’elles sont en phase de latence. Toutes ces raisons font qu’actuellement le traitement antituberculeux consiste à prendre tous les jours, pendant 3 à 6 mois minimum, plusieurs antibiotiques en même temps, ce afin d’augmenter les chances de toucher toutes les formes physiologiques de la bactérie présentes dans l’organisme.
Source : Inserm
« La tuberculose demeure compliquée à prévenir et d’autant plus complexe à traiter puisqu’elle devient résistante aux traitements antibiotiques, d’où les échecs des thérapies actuelles. Notre équipe a démontré contre toute attente que cette résistance n’est pas un phénomène irréversible. »
Deux solutions sont possibles pour lutter contre ce phénomène d’antibiorésistance. Une première solution, étudiée à l’Institut Pasteur de Lille, consiste à tenter de faire marche arrière sur la résistance par l’utilisation de molécules appelées « Boosters(3) ». Les chercheurs lillois, pionniers au niveau mondial dans ce domaine, ont démontré que la résistance n’est pas un phénomène irréversible, mais peut être réverté. Le projet baptisé TB-Boost sur lequel ils travaillent a permis de développer un Booster, actuellement en fin de phase I de son essai clinique. Cet essai s’est déroulé en Espagne, sur des personnes saines volontaires qui ont reçu à l’hôpital, sous surveillance médicale, des doses progressivement croissantes du Booster jusqu’à atteindre la dose utilisée pour le traitement, permettant ainsi de déterminer si les volontaires perçoivent des effets secondaires.
La phase II de l’essai clinique débutera en mars 2022 et permettra de mesurer l’efficacité de la molécule. Cet essai nécessite de recruter un nombre important de malades volontaires. Il sera déployé en Afrique du Sud où le taux de personnes atteintes par la tuberculose est un des plus élevés au monde (jusqu’à 1000 cas pour 100.000 habitants dans certaines villes). Il faut pour cet essai déterminer la dose efficace associant l’antibiotique (l’éthionamide) et le Booster, et qui ne provoque pas d’effet secondaire chez les patients malades.
Parallèlement à cet essai qui sera mené pour mesurer la révertance de la résistance de la bactérie à l’éthionamide grâce au Booster, les chercheurs de l’Institut Pasteur de Lille diversifient cette technique à d’autres antibiotiques plus récents comme le prétonamide mis sur le marché il y a deux ans, et pour lequel on commence déjà à voir apparaitre les premières résistances. Cette fois, les chercheurs généralisent la technologie TB-Boost à des molécules plus modernes en étudiant la possibilité de réussir non pas à réverter la résistance, mais à protéger l’apparition de ces résistances à l’aide d’une technologie Boost. La plateforme de criblage à haut débit dont dispose l’Institut Pasteur de Lille a permis d’avancer de manière beaucoup plus rapide.
Forts de toutes ces recherches sur l’antibiorésistance, notamment de la tuberculose, les chercheurs de l’Institut Pasteur de Lille ont répondu à l’appel à projets recherche “Antibiorésistance : comprendre, innover, agir” et les trois appels structurants, le Programme Prioritaire de Recherche (PPR) Antibiorésistance coordonné par l’Inserm et financé par le Programme d’Investissements d’Avenir (PIA), en collaboration avec l’Agence Nationale de la Recherche (ANR). Cet appel vise à développer une recherche d’excellence dans le domaine de l’antibiorésistance afin d’enrichir l’environnement et les infrastructures de recherche en cours de construction en France.
Le projet « Mustart », coordonné à l’échelle nationale par l’Institut Pasteur de Lille, regroupant sept puissantes équipes de recherche spécialisées dans la tuberculose (dont deux en milieu hospitalier) ainsi que deux partenaires d’autres domaines apportant des approches méthodologiques nouvelles, ambitionne de relever cet enjeu par des actions de recherche concertées et intégrées, allant du laboratoire au chevet du patient. En parallèle, le projet Mustart vise à identifier des biomarqueurs traduisant l’évolution du traitement en temps réel, chez un modèle et chez les patients. Ces marqueurs, destinés à prédire les rechutes et l’apparition de résistances, permettront de personnaliser les traitements de manière rationnelle et en temps réel.
D’autres travaux sont actuellement en cours à l’Institut Pasteur de Lille au sein du CIIL (Centre d’Infection et d’Immunité de Lille) sur l’antibiorésistance par le Dr Hartkoorn (Institut Pasteur de Lille, INSERM U1019 – CNRS UMR 9017, Université de Lille, CHU Lille) et son équipe qui travaillent sur le développement de nouvelles molécules pour lutter contre les bactéries pathogènes, et des outils contre la tuberculose et les bactéries nosocomiales(4).
A lire en complément :
Maladies émergentes et antibiorésistance :
Le Dr Sandrine Belouzard et le Dr Alain Baulard nous expliquent ces phénomènes
et nous parlent de leurs travaux de recherche à l’Institut Pasteur de Lille
INTHREPIDE : programme de lutte contre les risques épidémiologiques et l’antibiorésistance
Pour lutter contre ces phénomènes alarmants, les chercheurs d’Institut Pasteur de Lille mettent tout en œuvre grâce au programme INTHREPIDE : le programme de lutte contre les risques épidémiques et la résistance aux antibiotiques.
Les récentes pandémies montrent l’impérieuse nécessité pour nos sociétés de se donner les moyens d’une très grande réaction face à l’émergence d’agents pathogènes susceptibles de les déstabiliser. Le programme de recherche INTHREPIDE, lancé par les chercheurs de l’IPL a pour ambition d’identifier de nouveaux principes thérapeutiques contre les infections virales émergentes et les infections par des bactéries multi-résistantes.
AXE 1 : les infections virales
- Concevoir un antiviral contre les virus actuels connus et circulants, mais aussi contre toutes les espèces à risque d’émergence.
- Concevoir des antiviraux dirigés contre l’ensemble des virus de la famille des coronavirus.
AXE 2 : les infections bactériennes
- Identifier de nouveaux composés capables de potentialiser l’action d’antibiotiques existants en inhibant les mécanismes de résistance.
- Identifier de nouveaux antibiotiques visant les bactéries qui posent les plus grands problèmes de résistance.
Définitions
(1) Zoonoses : Les zoonoses sont des maladies ou infections qui se transmettent des animaux vertébrés à l’homme, et vice versa. Les pathogènes en cause peuvent être des bactéries, des virus ou des parasites.
(2) Macrophages : Cellule ayant la propriété d’ingérer et de détruire de grosses particules (cellules lésées ou vieillies, particules étrangères, bactéries) par phagocytose.
(3) Booster : Nom donné à une molécule ayant la faculté de de réactiver ou d’accélérer un processus enzymatique dans une bactérie et de réverter sa résistance à un antibiotique.
(4) Bactéries nosocomiales : Bactéries responsables des infections associées aux soins contractées au cours d’un séjour dans un établissement de soins. Elle peut être directement liée aux soins ou survenir durant l’hospitalisation, en dehors de tout acte médical.