La biologie structurale constitue un des socles indispensables de la médecine moderne. En cartographiant l’architecture intime des macromolécules, nous ne nous contentons pas d’observer le vivant ; nous décryptons les mécanismes fondamentaux qui permettent de concevoir les thérapies de demain. Cet entretien nous plonge au cœur des travaux du Pr Vincent Villeret, chercheur au CNRS. Biochimiste de formation avec trente ans d’expertise dans l’exploration moléculaire, il nous présente l’évolution technique de cette méthode, ses avantages pour l’étude de complexes protéiques flexibles et ses applications concrètes dans la recherche sur le cancer ou les maladies infectieuses. Au sein d’une unité de recherche mixte regroupant le CNRS, l’Institut Pasteur de Lille et l’Université de Lille, le chercheur et son équipe développent une approche intégrative pour traduire la complexité technologique en enjeux de santé publique.
Pr Vincent Villeret, chercheur au CNRS à l’Institut Pasteur de Lille

Pouvez-vous définir votre spécialité au sein de cette unité mixte et nous expliquer comment vos travaux ont évolué, notamment avec le virage technologique récent ?
Vincent Villeret (VV) : Ma spécialité est la biologie structurale intégrative. L’originalité de notre site lillois réside dans une triple expertise rare : la Résonance Magnétique Nucléaire (RMN), la cristallographie et, désormais, la cryo-microscopie électronique (Cryo-EM). Mon propre parcours est emblématique de cette mutation : historiquement cristallographe, j’ai pivoté vers la Cryo-EM au moment de la crise du Covid. Ce changement n’était pas un choix de confort, mais une nécessité scientifique. J’étais bloqué par les limites intrinsèques de la cristallographie pour répondre aux questions complexes que pose le système du “complexe du Médiateur”. Ce passage à la Cryo-EM nous a permis de franchir un mur technologique.
Quel est le principal progrès apporté à la recherche par la cryo-microscopie ?
VV : Pendant soixante ans, la cristallographie aux rayons X a été l’outil de référence. Cependant, elle impose un goulot d’étranglement majeur : l’obligation de transformer des protéines souples en cristaux rigides. La Cryo-EM brise ce verrou en permettant d’imager les molécules sans les cristalliser. Il s’agit d’une véritable révolution : en effet, les grandes fonctions biologiques sont majoritairement accomplies par des complexes macromoléculaires dynamiques de grande taille qui sont souvent restés, pendant des décennies, réfractaires à la cristallisation. La cryoEM permet à présent leur analyse structurale, dans un état proche de leur conformation native. Pour les systèmes membranaires, qui ne sont pas solubles hors phase détergent ou nanodisque, c’est également une révolution : ces systèmes représentent 50 % des cibles médicamenteuses actuelles, mais étaient historiquement presque impossibles à cristalliser.
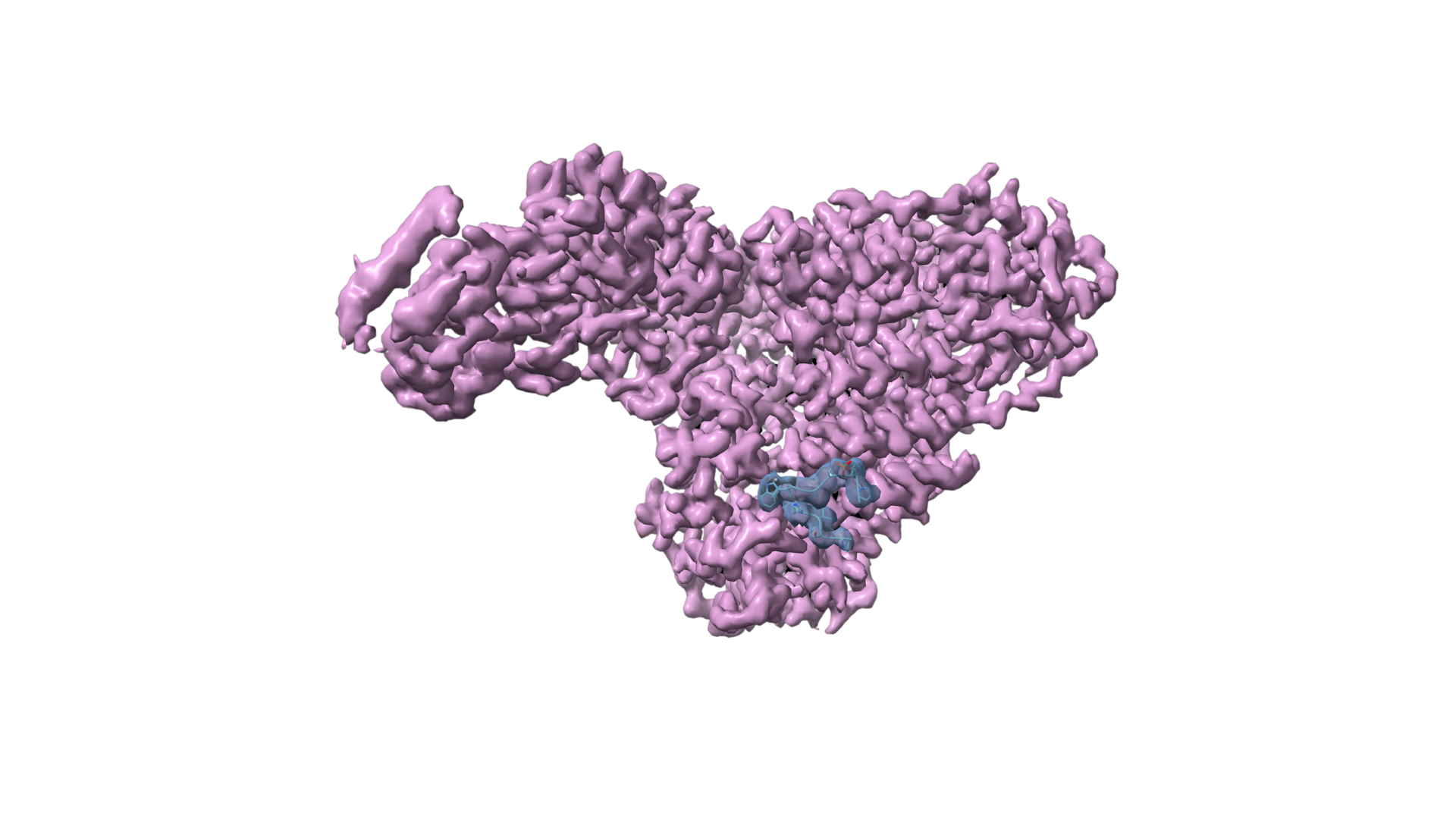
Quels obstacles technologiques la cryoEM a-t-elle permis de surmonter ?
VV : Bien que la microscopie électronique existe depuis les années 1930, son application à la haute résolution biologique a longtemps buté sur deux problèmes physiques qui ont été résolus par la “méthode cryo”. Le faisceau d’électrons circulant sous vide, les échantillons biologiques s’évaporaient instantanément. La solution est la vitrification : l’échantillon est plongé si rapidement dans l’éthane liquide (refroidi par azote liquide) que l’eau n’a pas le temps de cristalliser. Elle forme une “glace vitreuse” qui fige la structure sans la modifier. D’autre part, les électrons détruisent les liaisons chimiques. Pour contrer cela, nous travaillons à des doses d’électrons extrêmement faibles.
Avec des doses aussi faibles, le rapport signal sur bruit doit être très dégradé. Comment parvenez-vous à une précision atomique ?
VV : C’est le cœur de la révolution de 2012. L’apparition des dispositifs à détection directe d’électrons a radicalement changé la donne. En couplant ces capteurs à une puissance de calcul massive, nous imageons des milliers de fois la même particule sous différents angles. Les logiciels de traitement de données actuels permettent ensuite de reconstruire une structure 3D d’une précision atomique. C’est une symbiose parfaite entre physique du froid, optique électronique et algorithmique de pointe.
Quelles sont les principales applications pour lesquelles vous utilisez la Cryo-EM ?
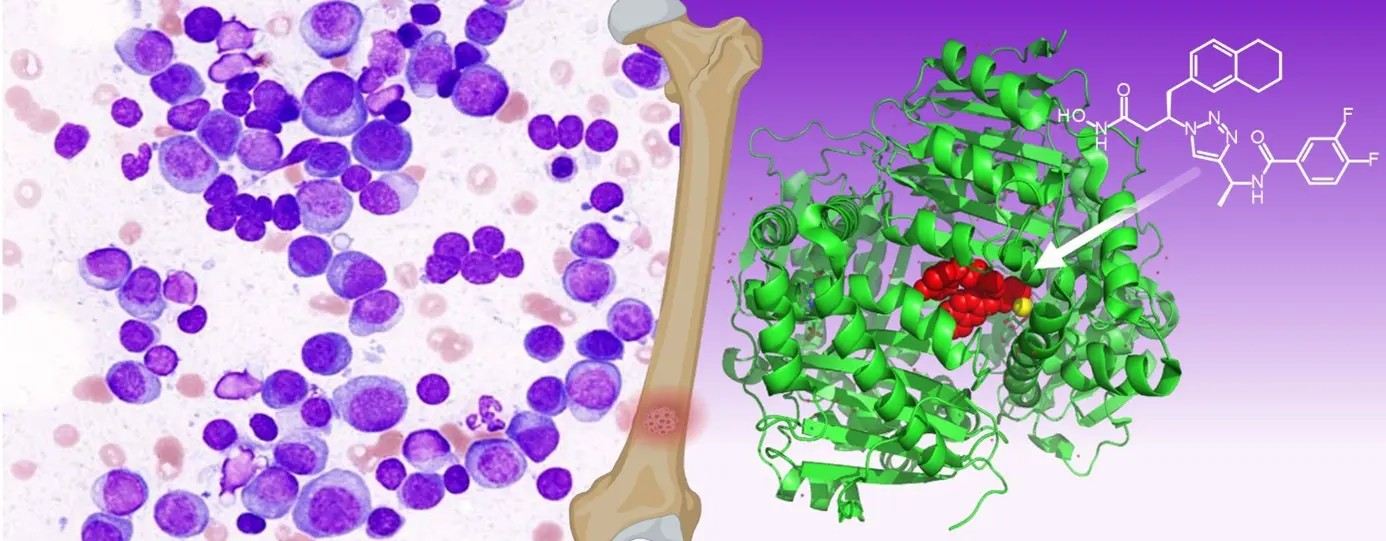
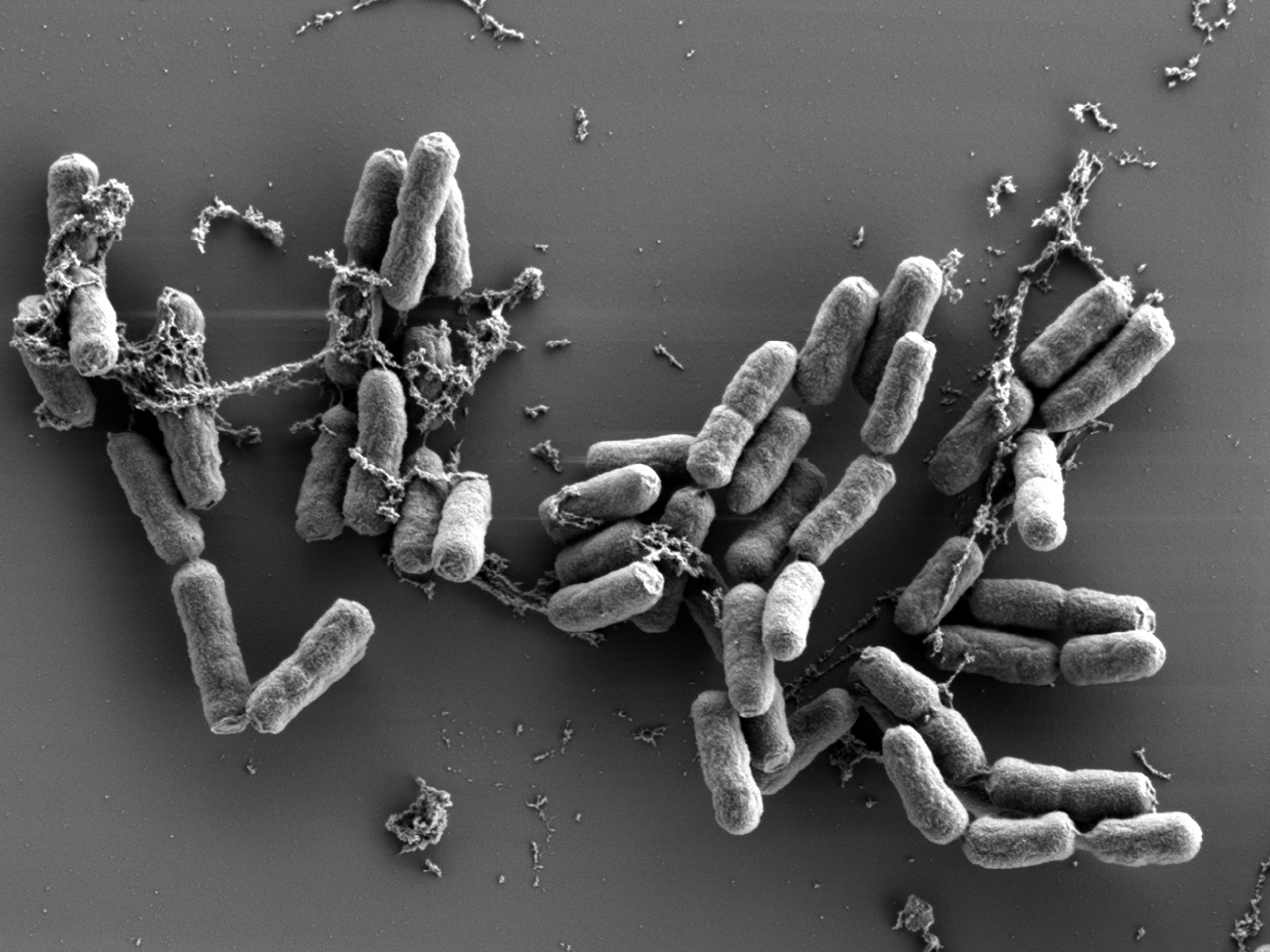
VV : L’impact de la Cryo-EM est immédiat pour la santé publique, comme en témoignent nos trois axes de recherche actuels. En neurologie et oncologie (transcription eucaryote) tout d’abord. Nous étudions comment les facteurs de transcription humains recrutent le complexe du Médiateur. Celui-ci est un constituant essentiel du complexe d’initiation de la transcription chez les organismes eucaryotes, une machinerie colossale de 80 protéines pesant 5 millions de daltons. Ces facteurs de transcription sont, pour la plupart, des oncogènes. Comprendre cette architecture, comme nous l’avons publié dans Nature Communications au printemps 2025, permet d’envisager de nouvelles cibles pour bloquer la progression tumorale. En bactériologie ensuite, dans le cadre d’une collaboration de 25 ans avec Françoise Jacob-Dubuisson, nous étudions les systèmes de virulence de la bactérie Bordetella pertussis (agent responsable de la Coqueluche). Nous utilisons la Cryo-EM pour cartographier les transporteurs membranaires tels que FHAC. Déterminer la structure de ces systèmes est une des clés pour mieux neutraliser la virulence bactérienne. Enfin en virologie, dans le cadre d’un projet porté par Xavier Hanoulle et Sandrine Belouzard, nous explorons les protéines de membrane des coronavirus. La Cryo-EM est ici l’outil providentiel pour étudier ces protéines non solubles et dynamiques. Ces travaux sont menés au sein de l’UMR 9031 nouvellement créée, sous la direction d’Isabelle Landrieu.
Qu’en est-il de l’enjeu Stratégique de l’équipement et du financement ?
VV : Si la France résorbe son retard national face à l’Allemagne ou aux États-Unis, la région des Hauts-de-France demeure un point mort technologique en matière de haute résolution. C’est un enjeu de souveraineté scientifique régionale. L’investissement nécessaire se structure en différents niveaux : La préparation tout d’abord avec l’acquisition d’un Vitrobot, représentant un investissement d’environ 50 000 €, qui nous permet de préparer les grilles cryogénisées au laboratoire. En second, la haute résolution avec un équipement de type Titan Krios (300 kV), summum technologique coûtant entre 5 et 7 millions d’euros. Ces machines sont disponibles sur des plateformes nationales ou européennes (Soleil, ESRF). Mais notre priorité est l’acquisition d’un microscope intermédiaire (1 à 1,5 million d’euros), maillon manquant à Lille. Cet outil n’est pas un luxe, mais une condition de viabilité économique et scientifique. Il est indispensable pour tester localement et obtenir des grilles cryogénisées de qualité. Sans lui, la mise au point des grilles est actuellement un processus chronophage et coûteux, nécessitant des déplacements hors de la région, ce qui freine notre compétitivité face à la concurrence internationale. Cette phase de mise au point est bien évidemment indispensable pour accéder aux plateformes nationales, où obtenir du temps de mesure est très compétitif et strictement contrôlé.
Au-delà de l’équipement, il s’agit de créer une émulation. La Cryo-EM est devenue une technique fondamentale de la biologie moléculaire moderne. En dotant la région de cette infrastructure intermédiaire, nous permettons au génie collectif de nos chercheurs de s’exprimer pleinement pour relever les défis sanitaires du XXIe siècle.